વિદ્યુત વિચ્છેદન-વિશ્લેષણ શું છે તે પ્રશ્ન શાળા ભૌતિકશાસ્ત્રના અભ્યાસક્રમમાં ગણવામાં આવે છે, અને મોટાભાગના લોકો માટે તે ગુપ્ત નથી. બીજી વસ્તુ તેનું મહત્વ અને વ્યવહારુ ઉપયોગ છે. આ પ્રક્રિયાનો ઉપયોગ વિવિધ ઉદ્યોગોમાં ખૂબ ફાયદા સાથે થાય છે અને ઘરના કારીગર માટે ઉપયોગી થઈ શકે છે.
સામગ્રી
- 1 વિદ્યુત વિચ્છેદન-વિશ્લેષણ શું છે?
- 2 વિદ્યુત વિચ્છેદન-વિશ્લેષણના ફેરાડેના નિયમો
- 3 મેલ્ટ વિદ્યુત વિચ્છેદન-વિશ્લેષણ
- 4 ઉકેલોમાં વિદ્યુત વિચ્છેદન-વિશ્લેષણની સુવિધાઓ
- 5 વાયુઓમાં ઇલેક્ટ્રોલિસિસ
- 6 કેથોડ અને એનોડ પર થતી પ્રક્રિયાઓની વિશેષતાઓ
- 7 વિદ્યુત વિચ્છેદન-વિશ્લેષણ પ્રક્રિયાને અસર કરતા પરિબળો
- 8 વિદ્યુત વિચ્છેદન-વિશ્લેષણ ક્યાં વપરાય છે?
- 9 ઊર્જા ખર્ચ
વિદ્યુત વિચ્છેદન-વિશ્લેષણ શું છે?
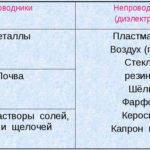
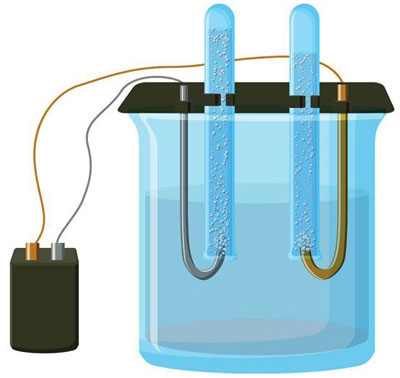
વિદ્યુત વિચ્છેદન-વિશ્લેષણ એ ઇલેક્ટ્રોડ્સ અને ઇલેક્ટ્રોલાઇટની સિસ્ટમમાં ચોક્કસ પ્રક્રિયાઓનું એક જટિલ છે જ્યારે તેમાંથી સીધો વિદ્યુત પ્રવાહ વહે છે. તેની પદ્ધતિ આયનીય પ્રવાહની ઘટના પર આધારિત છે. ઇલેક્ટ્રોલાઇટ એક પ્રકાર 2 વાહક છે (આયનીય વાહકતા) જેમાં ઇલેક્ટ્રોલાઇટિક વિયોજન થાય છે. તે સકારાત્મક સાથે આયનોમાં વિઘટન સાથે સંકળાયેલ છે (cation) અને નકારાત્મક (anion) ચાર્જ.
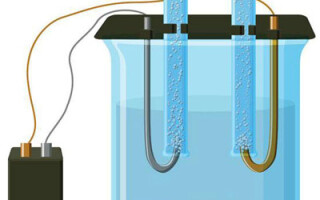
વિદ્યુત વિચ્છેદન-વિશ્લેષણ સિસ્ટમમાં આવશ્યકપણે હકારાત્મક (એનોડ) અને નકારાત્મક (કેથોડ) ઇલેક્ટ્રોડ. જ્યારે સીધો વિદ્યુત પ્રવાહ લાગુ થાય છે, ત્યારે કેશન્સ કેથોડ તરફ જવાનું શરૂ કરે છે, અને આયન - એનોડ તરફ. કેશન્સ મુખ્યત્વે ધાતુના આયનો અને હાઇડ્રોજન છે, અને આયન ઓક્સિજન, ક્લોરિન છે. કેથોડ પર, કેશન્સ વધારાના ઇલેક્ટ્રોનને પોતાની સાથે જોડે છે, જે ઘટાડાની પ્રતિક્રિયાની ઘટનાને સુનિશ્ચિત કરે છે Men+ + ne → Me (જ્યાં n એ ધાતુની વેલેન્સી છે). એનોડ પર, તેનાથી વિપરીત, ઓક્સિડેટીવ પ્રતિક્રિયા સાથે આયનમાંથી ઇલેક્ટ્રોનનું દાન કરવામાં આવે છે.
આમ, સિસ્ટમમાં રેડોક્સ પ્રક્રિયા પૂરી પાડવામાં આવે છે. તે ધ્યાનમાં લેવું મહત્વપૂર્ણ છે કે તેના પ્રવાહ માટે, યોગ્ય ઊર્જાની જરૂર છે. તે બાહ્ય વર્તમાન સ્ત્રોત દ્વારા પ્રદાન કરવું આવશ્યક છે.
વિદ્યુત વિચ્છેદન-વિશ્લેષણના ફેરાડેના નિયમો
મહાન ભૌતિકશાસ્ત્રી એમ. ફેરાડે, તેમના સંશોધન દ્વારા, માત્ર વિદ્યુત વિચ્છેદન-વિશ્લેષણની પ્રકૃતિને સમજવા માટે જ નહીં, પરંતુ તેના અમલીકરણ માટે જરૂરી ગણતરીઓ કરવાનું પણ શક્ય બનાવ્યું. 1832 માં, તેના કાયદાઓ દેખાયા, જે ચાલુ પ્રક્રિયાઓના મુખ્ય પરિમાણોને જોડે છે.
પ્રથમ કાયદો
ફેરાડેનો પ્રથમ કાયદો જણાવે છે કે એનોડ પર ઘટતા પદાર્થનું દળ ઇલેક્ટ્રોલાઇટમાં પ્રેરિત ઇલેક્ટ્રિક ચાર્જના સીધા પ્રમાણસર છે: m = kq = k*I*t, જ્યાં q એ ચાર્જ છે, k એ ગુણાંક અથવા ઇલેક્ટ્રોકેમિકલ સમકક્ષ છે પદાર્થની, I એ ઇલેક્ટ્રોલાઇટ દ્વારા વહેતા પ્રવાહની તાકાત છે, t એ વર્તમાન પસાર થવાનો સમય છે.

બીજો કાયદો
ફેરાડેના બીજા કાયદાએ પ્રમાણસરતા k નો ગુણાંક નક્કી કરવાનું શક્ય બનાવ્યું. તે આના જેવું લાગે છે: કોઈપણ પદાર્થની વિદ્યુતરાસાયણિક સમકક્ષ તેના દાઢ સમૂહના સીધા પ્રમાણસર હોય છે અને વેલેન્સીના વિપરિત પ્રમાણમાં હોય છે. કાયદો આ રીતે વ્યક્ત થાય છે:

k = 1/F*A/z, જ્યાં F એ ફેરાડે સ્થિરાંક છે, A એ પદાર્થનો દાઢ સમૂહ છે, z એ તેની રાસાયણિક વેલેન્સી છે.
બંને કાયદાઓને ધ્યાનમાં લેતા, પદાર્થના ઇલેક્ટ્રોડ પર જમા થયેલ સમૂહની ગણતરી માટે અંતિમ સૂત્ર મેળવવાનું શક્ય છે: m = A*I*t/(n*F), જ્યાં n એ વિદ્યુત વિચ્છેદન-વિશ્લેષણમાં સામેલ ઇલેક્ટ્રોનની સંખ્યા છે. સામાન્ય રીતે n આયનના ચાર્જને અનુલક્ષે છે. વ્યવહારિક દૃષ્ટિકોણથી, પદાર્થના સમૂહ અને લાગુ પ્રવાહ વચ્ચેનું જોડાણ મહત્વપૂર્ણ છે, જે તેની શક્તિને બદલીને પ્રક્રિયાને નિયંત્રિત કરવાનું શક્ય બનાવે છે.
મેલ્ટ વિદ્યુત વિચ્છેદન-વિશ્લેષણ
વિદ્યુત વિચ્છેદન-વિશ્લેષણ માટેના વિકલ્પોમાંનો એક ઇલેક્ટ્રોલાઇટ તરીકે મેલ્ટનો ઉપયોગ છે. આ કિસ્સામાં, માત્ર ઓગળેલા આયનો વિદ્યુત વિચ્છેદન પ્રક્રિયામાં ભાગ લે છે. એક ઉત્તમ ઉદાહરણ પીગળેલા મીઠાનું વિદ્યુત વિચ્છેદન છે NaCl (મીઠું). નકારાત્મક આયનો એનોડ તરફ ધસી જાય છે, જેનો અર્થ છે કે ગેસ છોડવામાં આવે છે (Cl). કેથોડ પર મેટલ ઘટાડો થશે, એટલે કે. સકારાત્મક આયનોમાંથી રચાયેલ શુદ્ધ Na નું જુબાની કે જે વધારાના ઇલેક્ટ્રોનને આકર્ષે છે. અન્ય ધાતુઓ એ જ રીતે મેળવી શકાય છે (K, Ca, Li, વગેરે.) અનુરૂપ ક્ષારના હત્યાકાંડમાંથી.
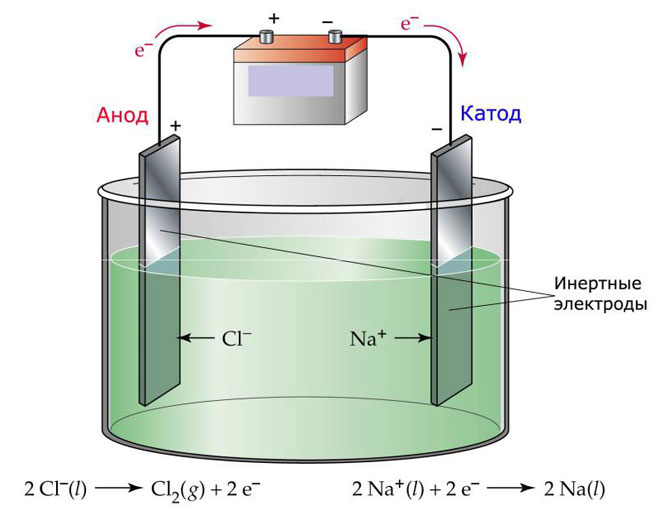
મેલ્ટમાં વિદ્યુત વિચ્છેદન-વિશ્લેષણ દરમિયાન, ઇલેક્ટ્રોડ્સ વિસર્જનમાંથી પસાર થતા નથી, પરંતુ માત્ર વર્તમાન સ્ત્રોત તરીકે ભાગ લે છે. તેમના ઉત્પાદનમાં, તમે મેટલ, ગ્રેફાઇટ, કેટલાક સેમિકન્ડક્ટરનો ઉપયોગ કરી શકો છો. તે મહત્વનું છે કે સામગ્રીમાં પૂરતી વાહકતા છે. સૌથી સામાન્ય સામગ્રીમાંની એક તાંબુ છે.
ઉકેલોમાં વિદ્યુત વિચ્છેદન-વિશ્લેષણની સુવિધાઓ
જલીય દ્રાવણમાં વિદ્યુત વિચ્છેદન-વિશ્લેષણ મેલ્ટ કરતા નોંધપાત્ર રીતે અલગ પડે છે. અહીં ત્રણ સ્પર્ધાત્મક પ્રક્રિયાઓ થાય છે: ઓક્સિજન ઉત્ક્રાંતિ સાથે પાણીનું ઓક્સિડેશન, આયન ઓક્સિડેશન અને ધાતુનું એનોડિક વિસર્જન. પાણીના આયનો, ઇલેક્ટ્રોલાઇટ અને એનોડ પ્રક્રિયામાં સામેલ છે.તદનુસાર, કેથોડ પર હાઇડ્રોજન, ઇલેક્ટ્રોલાઇટ કેશન અને એનોડ મેટલનો ઘટાડો થઈ શકે છે.

આ સ્પર્ધાત્મક પ્રક્રિયાઓ થવાની સંભાવના સિસ્ટમની વિદ્યુત સંભવિતતાઓની તીવ્રતા પર આધારિત છે. માત્ર તે જ પ્રક્રિયા આગળ વધશે જેને ઓછી બાહ્ય ઊર્જાની જરૂર હોય. પરિણામે, કેથોડ પર મહત્તમ ઇલેક્ટ્રોડ સંભવિત સાથેના કેશનમાં ઘટાડો થશે, અને સૌથી ઓછી સંભવિતતાવાળા આયનોને એનોડ પર ઓક્સિડાઇઝ કરવામાં આવશે. હાઇડ્રોજનના ઇલેક્ટ્રોડ સંભવિતને "0" તરીકે લેવામાં આવે છે. ઉદાહરણ તરીકે, પોટેશિયમ માટે તે છે (-2.93V), સોડિયમ - (-2.71V), લીડ (-0.13 વી), જ્યારે ચાંદીમાં (+0.8 વી).
વાયુઓમાં ઇલેક્ટ્રોલિસિસ
આયનાઇઝરની હાજરીમાં જ ગેસ ઇલેક્ટ્રોલાઇટની ભૂમિકા ભજવી શકે છે. આ કિસ્સામાં, આયનાઇઝ્ડ માધ્યમમાંથી પસાર થતો પ્રવાહ ઇલેક્ટ્રોડ્સ પર જરૂરી પ્રક્રિયાનું કારણ બને છે. જો કે, ફેરાડેના નિયમો ગેસ વિદ્યુત વિચ્છેદન-વિશ્લેષણ પર લાગુ પડતા નથી. તેના અમલીકરણ માટે, નીચેની શરતો આવશ્યક છે:
- ગેસના કૃત્રિમ આયનીકરણ વિના, ન તો ઉચ્ચ વોલ્ટેજ કે ઉચ્ચ પ્રવાહ મદદ કરશે.
- માત્ર એસિડ કે જેમાં ઓક્સિજન નથી અને તે વાયુયુક્ત સ્થિતિમાં છે અને કેટલાક વાયુઓ વિદ્યુત વિચ્છેદન માટે યોગ્ય છે.
મહત્વપૂર્ણ! જ્યારે જરૂરી શરતો પૂરી થાય છે, ત્યારે પ્રક્રિયા પ્રવાહી ઇલેક્ટ્રોલાઇટમાં વિદ્યુત વિચ્છેદન-વિશ્લેષણની જેમ જ આગળ વધે છે.
કેથોડ અને એનોડ પર થતી પ્રક્રિયાઓની વિશેષતાઓ
વિદ્યુત વિચ્છેદન-વિશ્લેષણના વ્યવહારુ ઉપયોગ માટે, જ્યારે વિદ્યુત પ્રવાહ લાગુ કરવામાં આવે ત્યારે બંને ઇલેક્ટ્રોડ પર શું થાય છે તે સમજવું મહત્વપૂર્ણ છે. લાક્ષણિક પ્રક્રિયાઓ છે:
- કેથોડ. હકારાત્મક રીતે ચાર્જ થયેલા આયનો તેની તરફ ધસી આવે છે. અહીં, ધાતુઓમાં ઘટાડો અથવા હાઇડ્રોજનની ઉત્ક્રાંતિ થાય છે. કેશનિક પ્રવૃત્તિ અનુસાર ધાતુઓની ઘણી શ્રેણીઓ છે.Li, K, Ba, St, Ca, Na, Mg, Be, Al જેવી ધાતુઓ માત્ર પીગળેલા ક્ષારમાંથી સારી રીતે ઓછી થાય છે. જો સોલ્યુશનનો ઉપયોગ કરવામાં આવે છે, તો પાણીના વિદ્યુત વિચ્છેદનને કારણે હાઇડ્રોજન છોડવામાં આવે છે. નીચેની ધાતુઓ - Mn, Cr, Zn, Fe, Cd, Ni, Ti, Co, Mo, Sn, Pb માટે દ્રાવણમાં ઘટાડો હાંસલ કરવો શક્ય છે, પરંતુ કેશનની પૂરતી સાંદ્રતા સાથે. Ag, Cu, Bi, Pt, Au, Hg માટે પ્રક્રિયા સૌથી સરળતાથી આગળ વધે છે.
- એનોડ. નકારાત્મક રીતે ચાર્જ થયેલ આયનો આ ઇલેક્ટ્રોડમાં પ્રવેશ કરે છે. ઓક્સિડાઇઝ્ડ, તેઓ મેટલમાંથી ઇલેક્ટ્રોન લે છે, જે તેમના એનોડિક વિસર્જન તરફ દોરી જાય છે, એટલે કે. સકારાત્મક ચાર્જ આયનોમાં સંક્રમણ, જે કેથોડને મોકલવામાં આવે છે. Anions પણ તેમની પ્રવૃત્તિ અનુસાર વર્ગીકૃત કરવામાં આવે છે. આવા anions PO4, CO3, SO4, NO3, NO2, ClO4, F માત્ર ઓગળવાથી જ છૂટા થઈ શકે છે. જલીય દ્રાવણમાં, તે વિદ્યુત વિચ્છેદન-વિશ્લેષણમાંથી પસાર થતા નથી, પરંતુ ઓક્સિજનના પ્રકાશન સાથે પાણી છે. આયનો જેમ કે OH, Cl, I, S, Br સૌથી સરળતાથી પ્રતિક્રિયા આપે છે.

વિદ્યુત વિચ્છેદન-વિશ્લેષણની ખાતરી કરતી વખતે, ઇલેક્ટ્રોડ સામગ્રીની ઓક્સિડાઇઝ કરવાની વૃત્તિ ધ્યાનમાં લેવી મહત્વપૂર્ણ છે. આ સંદર્ભે, નિષ્ક્રિય અને સક્રિય એનોડ અલગ પડે છે. નિષ્ક્રિય ઇલેક્ટ્રોડ ગ્રેફાઇટ, કાર્બન અથવા પ્લેટિનમના બનેલા હોય છે અને આયનોના પુરવઠામાં ભાગ લેતા નથી.
વિદ્યુત વિચ્છેદન-વિશ્લેષણ પ્રક્રિયાને અસર કરતા પરિબળો
વિદ્યુત વિચ્છેદન-વિશ્લેષણ પ્રક્રિયા નીચેના પરિબળો પર આધારિત છે:
- ઇલેક્ટ્રોલાઇટ રચના. વિવિધ અશુદ્ધિઓ નોંધપાત્ર અસર કરે છે. તેઓ 3 પ્રકારોમાં વહેંચાયેલા છે - કેશન, આયન અને ઓર્ગેનિક્સ. પદાર્થો બેઝ મેટલ કરતાં વધુ કે ઓછા નકારાત્મક હોઈ શકે છે, જે પ્રક્રિયામાં દખલ કરે છે. કાર્બનિક અશુદ્ધિઓમાં, પ્રદૂષકો (દા.ત. તેલ) અને સર્ફેક્ટન્ટ અલગ પડે છે. તેમની સાંદ્રતામાં મહત્તમ અનુમતિપાત્ર મૂલ્યો છે.
- વર્તમાન ઘનતા. ફેરાડેના કાયદા અનુસાર, જમા થયેલ પદાર્થનો સમૂહ વર્તમાન શક્તિમાં વધારો સાથે વધે છે. જો કે, બિનતરફેણકારી સંજોગો ઉભા થાય છે - કેન્દ્રિત ધ્રુવીકરણ, વોલ્ટેજમાં વધારો, ઇલેક્ટ્રોલાઇટની તીવ્ર ગરમી. આને ધ્યાનમાં રાખીને, દરેક ચોક્કસ કેસ માટે શ્રેષ્ઠ વર્તમાન ઘનતા મૂલ્યો છે.
- ઇલેક્ટ્રોલાઇટ pH. પર્યાવરણની એસિડિટી પણ ધાતુઓને ધ્યાનમાં રાખીને પસંદ કરવામાં આવે છે. ઉદાહરણ તરીકે, ઝીંક માટે ઇલેક્ટ્રોલાઇટ એસિડિટીનું શ્રેષ્ઠ મૂલ્ય 140 g/cu.dm છે.
- ઇલેક્ટ્રોલાઇટ તાપમાન. તેની અસ્પષ્ટ અસર છે. તાપમાનમાં વધારા સાથે, વિદ્યુત વિચ્છેદન-વિશ્લેષણનો દર વધે છે, પરંતુ અશુદ્ધિઓની પ્રવૃત્તિ પણ વધે છે. દરેક પ્રક્રિયા માટે મહત્તમ તાપમાન હોય છે. સામાન્ય રીતે તે 38-45 ડિગ્રીની રેન્જમાં હોય છે.
મહત્વપૂર્ણ! વિવિધ પ્રભાવો અને ઇલેક્ટ્રોલાઇટ રચનાની પસંદગી દ્વારા વિદ્યુત વિચ્છેદન-વિશ્લેષણને ઝડપી અથવા ધીમી કરી શકાય છે. દરેક એપ્લિકેશનની પોતાની પદ્ધતિ હોય છે, જેનું સખતપણે અવલોકન કરવું આવશ્યક છે.
વિદ્યુત વિચ્છેદન-વિશ્લેષણ ક્યાં વપરાય છે?
ઇલેક્ટ્રોલિસિસનો ઉપયોગ ઘણા ક્ષેત્રોમાં થાય છે. વ્યવહારુ પરિણામો મેળવવા માટે ઉપયોગના ઘણા મુખ્ય ક્ષેત્રો છે.
ઇલેક્ટ્રોપ્લેટિંગ
ધાતુની પાતળી, ટકાઉ પ્લેટિંગ વિદ્યુત વિચ્છેદન-વિશ્લેષણ દ્વારા લાગુ કરી શકાય છે. કોટેડ કરવા માટેનું ઉત્પાદન કેથોડના સ્વરૂપમાં સ્નાનમાં સ્થાપિત થયેલ છે, અને ઇલેક્ટ્રોલાઇટમાં ઇચ્છિત ધાતુનું મીઠું હોય છે. તેથી તમે ઝીંક, ક્રોમિયમ અથવા ટીન સાથે સ્ટીલને આવરી શકો છો.

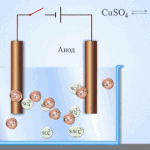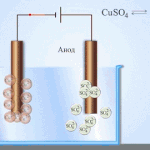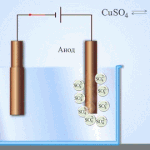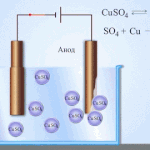
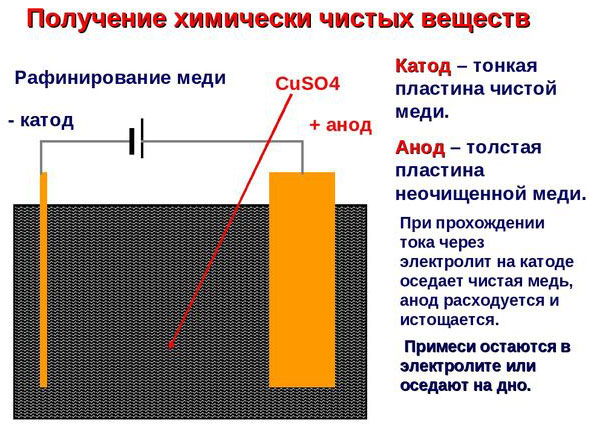
ઇલેક્ટ્રોરિફાઇનિંગ - કોપર રિફાઇનિંગ
વિદ્યુત સફાઈનું ઉદાહરણ નીચેના વિકલ્પ હોઈ શકે છે: કેથોડ - શુદ્ધ તાંબુ એનોડ - અશુદ્ધિઓ સાથે તાંબુ, ઇલેક્ટ્રોલાઇટ - કોપર સલ્ફેટનું જલીય દ્રાવણ. એનોડમાંથી તાંબુ આયનોમાં જાય છે અને અશુદ્ધિઓ વિના પહેલેથી જ કેથોડમાં સ્થાયી થાય છે.
મેટલ માઇનિંગ
ક્ષારમાંથી ધાતુઓ મેળવવા માટે, તેઓ ઓગળવામાં સ્થાનાંતરિત થાય છે, અને પછી તેમાં વિદ્યુત વિચ્છેદન-વિશ્લેષણ પ્રદાન કરવામાં આવે છે. બોક્સાઈટ્સ, સોડિયમ અને પોટેશિયમમાંથી એલ્યુમિનિયમ મેળવવા માટે આવી પદ્ધતિ તદ્દન અસરકારક છે.

એનોડાઇઝિંગ
આ પ્રક્રિયામાં, કોટિંગ બિન-ધાતુ સંયોજનોમાંથી બનાવવામાં આવે છે. એક ઉત્તમ ઉદાહરણ એલ્યુમિનિયમ એનોડાઇઝિંગ છે. એલ્યુમિનિયમ ભાગ એનોડ તરીકે સ્થાપિત થયેલ છે. ઇલેક્ટ્રોલાઇટ એ સલ્ફ્યુરિક એસિડનું દ્રાવણ છે. વિદ્યુત વિચ્છેદન-વિશ્લેષણના પરિણામે, એલ્યુમિનિયમ ઓક્સાઇડનો એક સ્તર એનોડ પર જમા થાય છે, જે રક્ષણાત્મક અને સુશોભન ગુણધર્મો ધરાવે છે. આ તકનીકોનો વ્યાપકપણે વિવિધ ઉદ્યોગોમાં ઉપયોગ થાય છે. તમે સલામતીના નિયમોનું પાલન કરીને તમારા પોતાના હાથથી પ્રક્રિયાઓ હાથ ધરી શકો છો.
ઊર્જા ખર્ચ
ઇલેક્ટ્રોલિસિસ માટે ઉચ્ચ ઊર્જા ખર્ચની જરૂર છે. જો એનોડ પ્રવાહ પૂરતો હોય તો પ્રક્રિયા વ્યવહારુ મૂલ્યની હશે, અને આ માટે પાવર સ્ત્રોતમાંથી નોંધપાત્ર સીધો પ્રવાહ લાગુ કરવો જરૂરી છે. વધુમાં, જ્યારે તે હાથ ધરવામાં આવે છે, ત્યારે બાજુના વોલ્ટેજનું નુકસાન થાય છે - એનોડ અને કેથોડ ઓવરવોલ્ટેજ, તેના પ્રતિકારને કારણે ઇલેક્ટ્રોલાઇટમાં નુકસાન. ઇન્સ્ટોલેશનની કાર્યક્ષમતા ઊર્જા વપરાશની શક્તિને પ્રાપ્ત પદાર્થના ઉપયોગી સમૂહના એકમ સાથે સંબંધિત કરીને નક્કી કરવામાં આવે છે.
ઇલેક્ટ્રોલિસિસનો ઉપયોગ ઉદ્યોગમાં લાંબા સમયથી અને ઉચ્ચ કાર્યક્ષમતા સાથે કરવામાં આવે છે. એનોડાઇઝ્ડ અને ઇલેક્ટ્રોપ્લેટેડ કોટિંગ્સ રોજિંદા જીવનમાં સામાન્ય બની ગયા છે, અને સામગ્રીનું ખાણકામ અને લાભો અયસ્કમાંથી ઘણી ધાતુઓ કાઢવામાં મદદ કરે છે. પ્રક્રિયાનું આયોજન અને ગણતરી કરી શકાય છે, તેના મુખ્ય પેટર્નને જાણીને.
સમાન લેખો: